1.アミノ酸の代謝
アミノ酸には、分子内にアミノ基(-NH2)の形で窒素が含まれています。そのため、アミノ酸の代謝においては、まずアミノ酸内の窒素を代謝する過程が重要になります。アミノ酸内の窒素の代謝に関わる反応には、主に2つの種類があります。
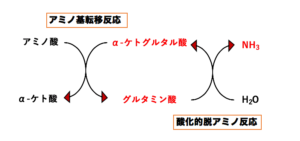
- アミノ基転移酵素(アミノトランスフェラーゼ)によるアミノ基転移反応
- アンモニア分子として取り除く酸化的脱アミノ反応
前者の反応では、既にアミノ基をもつ別のアミノ酸が必要であるという点が、後者の反応とは大きく異なっています。ちなみに、後者の反応としては、「グルタミン酸デヒドロゲナーゼ」と呼ばれるグルタミン酸の分解と合成の両方を担う酵素がアミノ酸代謝において特に重要になります。
2.アミノ基転移反応
アミノ基転移反応とは、アミノ基転移酵素(アミノトランスフェラーゼ)によって、アミノ酸とα-ケト酸との間でアミノ基が転移する反応のことです。すなわち、アミノ酸のもつアミノ基がα-ケト酸へと転移し、アミノ酸は対応するα-ケト酸に変換され、アミノ基を受け取ったα-ケト酸が対応するアミノ酸へと変換される反応になります。
※α-ケト酸とは、カルボキシル基の隣の位置にある炭素(α炭素)がケトン基(R−CO−R')になっている基質のことをいいます。ちなみに、アミノ酸からアミノ基が取り除かれると、アミノ酸は対応するα-ケト酸へと変化します。
アミノ基を受け取るα-ケト酸としては、主にα-ケトグルタル酸が用いられます。α-ケトグルタル酸はアミノ基転移反応によってアミノ基を受け取ると、グルタミン酸へと変換されます。
ほとんどのアミノ基転移反応のα-ケト酸として、α-ケトグルタル酸が用いられる理由は、対応するアミノ酸であるグルタミン酸が酸化的脱アミノ反応を受けて、アミノ基をアンモニア分子として遊離させることができるためと考えられます。
例えば、アラニンとオキサロ酢酸(アスパラギン酸に対応するα-ケト酸)との間でアミ ノ基が転移される反応では、これらのアミノ酸の間で直接アミノ基が転移されるのではなく、一旦、アラニンのアミノ基がα-ケトグルタル酸へと転移し、生じたグルタミン酸のアミノ基をオキサロ酢酸へと転移することで間接的にアスパラギン酸に転移されるという反応が行われます。
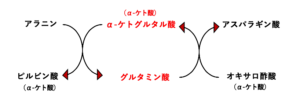
このようにして生じたα-ケト酸は、炭素骨格代謝を受け、グルタミン酸は酸化的脱アミノ反応を受けることによって代謝されます。
※α-ケト酸の炭素骨格代謝ついては「4)アミノ酸の炭素骨格の代謝(糖原性アミノ酸とケト原性アミノ酸の代謝)」で、グルタミン酸の酸化的脱アミノ反応については「2)グルタミン酸とグルタミンを介したアンモニアの体内輸送」で詳しく解説しています。
ヒトの体内で合成できる非必須アミノ酸のほとんどは、このアミノ基転移反応によって、対応するα-ケト酸から合成されています。また、体内では合成できない必須アミノ酸でも、外部から対応するα-ケト酸を取り入れることによって必須アミノ酸を体内で合成することは可能になります。
※一般的に、必須アミノ酸に対応するα-ケト酸は体内では生成されないため、必須アミノ酸を体内で合成できません。
※必須アミノ酸の種類と覚え方については「3)代表的なアミノ酸の分類(糖原性/ケト原性アミノ酸)」で詳しく解説しています。
3.アミノ基転移反応の補酵素
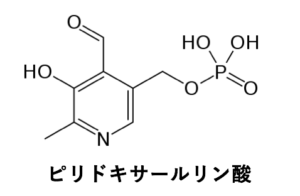
アミノ基転移反応では、補酵素としてピリドキサールリン酸(ビタミンB6)が必要になります。ピリドキサールリン酸はビタミンB6の活性型のことで、アミノトランスフェラーゼの活性中心にあるリシン残基のε-アミノ基とシッフ塩基(-C=N-)を形成して結合しています。
アミノ基転移反応の基質となるアミノ酸がアミノトランスフェラーゼの活性中心に近づくと、アミノ酸のアミノ基がリシン残基のε-アミノ基と入れ替わり、シッフ塩基を形成します。
その後、シッフ塩基を形成していたアミノ酸がα-ケト酸として遊離し、アミノ酸に由来するアミノ基はピリドキサールリン酸に結合した状態で残ります。この状態でアミノ基を受け取る別の α-ケト酸が近くことにより、α-ケト酸がピリドキサールリン酸に結合していたアミノ基を受け取り、対応するアミノ酸へと変換されます。
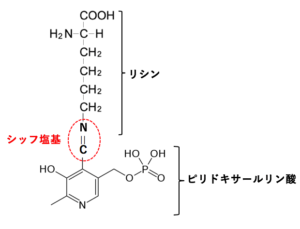
※シッフ塩基とは、アミノ基(-NH2)とアルデヒド基(-CHO)またはケトン基(-CO-)の間に形成される構造(-C=N-)のことをいいます。
アミノ基転移反応についてはこれで以上です。
次は「2)グルタミン酸とグルタミンを介したアンモニアの体内輸送」について学んでいきましょう。
-
-
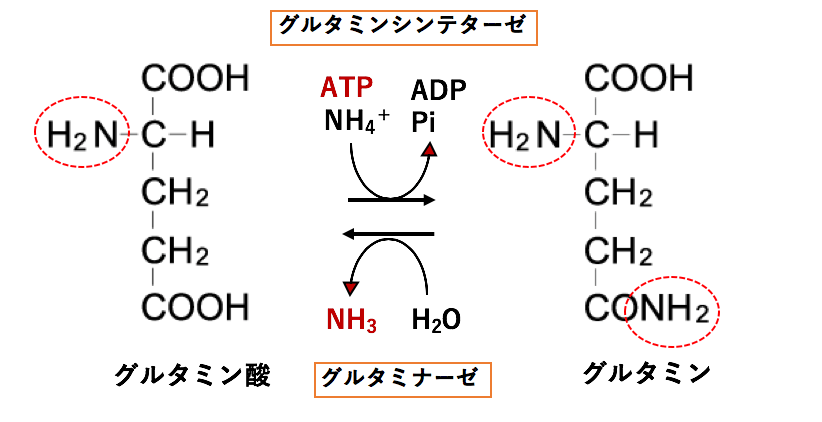
2)グルタミン酸とグルタミンを介したアンモニアの体内輸送
1.アミノ酸の代謝 アミノ酸には、分子内にアミノ基(-NH3)の形で窒素が含まれています。そのため、アミノ酸の代謝においては、まずアミノ酸内の窒素を代謝する過程が重要になります。アミノ酸内の窒素の代 ...
続きを見る